“La plupart des amateurs ont déjà lu ou entendu parler de l’importance du pH dans leur aquarium. Cependant, beaucoup d’entre nous ne comprennent pas vraiment ce concept ou son rôle fondamental dans la santé des organismes aquatiques”.
C’est pourquoi nous allons aborder aujourd’hui cet aspect si familier et pourtant si mal compris de la qualité de l’eau, mais surtout le véritable rôle qu’elle joue dans notre aquarium. Vous êtes prêts ?
Qu’est-ce que le pH ?

Où obtenons-nous ces valeurs pour déterminer le pH ?
C’est ici que l’explication se complique un peu. Lorsque nous parlons de pH, nous nous référons en fait à la concentration d’ions hydrogène chargés positivement dans une solution, appelés ions hydronium. La formule mathématique permettant de calculer le pH est le logarithme négatif en base 10 de l’activité des ions hydrogène. pH = -log10 [aH+]. En d’autres termes, une substance sera d’autant plus acide que son activité en ions hydrogène chargés positivement sera élevée. Inversement, lorsque l’activité est moindre, la substance est plus alcaline.
Pourquoi est-il important de savoir que la valeur du pH est une expression logarithmique ?
Nous sommes très habitués à mesurer la température de l’eau à l’aide de l’échelle Celsius, où, par exemple, une valeur de 10°C est deux fois plus froide qu’une valeur de 20°C, car ces valeurs forment une échelle linéaire ou géométrique. Cependant, si nous examinons la formule du pH, nous verrons que nous avons affaire à une expression logarithmique. Cela signifie qu’un pH de 7,0 est neutre, mais qu’il est dix fois plus acide qu’un pH de 8,0, cent fois plus acide qu’un pH de 9 , 0, mille fois plus acide qu’un pH de 10,0, etc.
“Il est important de maintenir un pH plus ou moins neutre, entre 6 et 8.
En réalité, cette phrase se réfère à un gradient dont la différence est jusqu’à 100 fois supérieure, ce qui est trop imprécis pour les exigences de qualité de l’eau dans n’importe quel aquarium. C’est comme si vous disiez :“Il est important de maintenir l’eau chaude, entre 0 °C et 100 °C.”
“Nous devons faire attention à la valeur du pH de notre aquarium, en la mesurant avec toute la précision et l’exactitude dont nous disposons”.
Le pH est un paramètre physique.
Les paramètres chimiques tels que la dureté (GH), les nitrites (NO2), les phosphates (PO₄³-) ou l’oxygène dissous (O2) indiquent la concentration de divers éléments ou composés dissous dans l’eau, ce qui est très utile pour déterminer la qualité de l’eau. En revanche, les paramètres physiques tels que le pH, la température, la densité, la conductivité ou le potentiel REDOX indiquent l’état de l’eau, à savoir si elle est acide ou alcaline, oxydante ou réductrice, chaude ou froide, dense ou fluide, conductrice ou isolante, etc. Les paramètres physiques ont également pour caractéristique d’influencer tous les autres paramètres, qu’ils soient physiques ou chimiques, et le pH ne fait pas exception. Prenons l’un des exemples les plus marquants pour comprendre l’importance du pH dans notre aquarium :Influence sur la toxicité de l’ammoniac/ammonium dans l’eau.
L’ammonium présent dans l’eau d’un aquarium provient des excrétions des poissons et d’autres déchets organiques, tels que les tissus végétaux en décomposition. La présence d’ammonium déclenche le processus bactérien connu sous le nom de “cycle de l’azote”. Lorsque l’azote (N) est présent dans l’eau (H2O), il peut se combiner avec l’hydrogène (H+ / OH-) pour former soit de l’ammoniac (NH3), soit de l’ammonium (NH4+), en fonction du pH de l’aquarium. Si le pH est acide, l’azote se combine pour former NH4+, tandis que s’il est alcalin, il forme NH3. Ce facteur est essentiel pour déterminer la toxicité de l’eau, car l’ammoniac est 200 à 300 fois plus toxique que l’ammonium. (Hinton DE, Laurén DJ, 1992)
“Pendant le cycle, il est préférable pour les aquariums de maintenir un pH inférieur à 7,0, car les niveaux d’ammoniaque seront élevés pendant les premiers jours.L’exception concerne les aquariums dont les habitants ont besoin d’un pH alcalin, comme les aquariums d’eau salée, d’eau saumâtre ou les cichlidés africains. Voyons ce qu’il en est :
L’importance du pH sur les organismes de la vie aquatique.
Spicules, thalles, squelettes, coquilles, épines et dents.
À de rares exceptions près, comme les tuniciers (ascidies), la plupart des organismes aquatiques ont besoin de produire du carbonate de calcium (CaCO3) pour construire leurs tissus rigides, essentiels à leur défense et à diverses fonctions vitales. Cependant, ce minéral réagit en se dissolvant dans l’eau lorsque le pH descend en dessous de 7,8. Cela entrave la création de nouveaux tissus et affaiblit sérieusement les tissus déjà formés. Ce syndrome de décalcification est particulièrement critique chez les organismes adaptés à la vie en eaux alcalines.Métabolisme et santé des poissons.
Nous savons que tous les poissons n’ont pas la même tolérance aux variations de pH, mais nous devons garder à l’esprit que si nous nous écartons de cette fourchette, des problèmes de santé ne tarderont pas à apparaître. Voyons pourquoi : À moyen terme, un pH trop acide entraîne des problèmes de dépôts de calcium dans les reins (néphrocalcinose) et de décalcification des tissus durs. Il affecte également la croissance en raison de problèmes d’appétit et d’absorption des nutriments.“Les effets les plus immédiats d’une valeur de pH inappropriée sur les poissons sont la réduction de leur efficacité respiratoire et de la capacité de leur système d’osmorégulation.
Le syndrome d’acidose.
À court terme, un pH trop bas entraîne une diminution drastique de la capacité de l’hémoglobine sanguine à absorber l’oxygène (effet Bohr, Wedemeyer, 1996). Cela conduit à un excès de CO2 dans le sang (hypercapnie) et à une diminution conséquente du pH (le sang des poissons se situe entre 7,7 et 8,0). En conséquence, le poisson affecté peut devenir léthargique, haleter à la surface de l’eau et présenter une respiration accélérée.

Le pH dans un aquarium planté.
Pendant la journée, les plantes aquatiques absorbent du dioxyde de carbone (CO2) et libèrent de l’oxygène (O2) au cours de la photosynthèse, ce qui augmente le pH. À l’inverse, la nuit, elles inversent ce processus, respirant l’O2 et libérant duCO2, qui réagit avec l’eau pour former de l’acide carbonique (H₂CO₃), abaissant ainsi le pH. Dans un environnement confiné comme un aquarium, le métabolisme des plantes aquatiques modifiera gravement le pH de l’aquarium par cycles de 12 heures s’il n’y a pas suffisamment de minéraux tampons comme les carbonates (KH). L’importance du pH dans notre aquarium planté est encore plus cruciale si nous voulons réussir notre projet. Le carbone nécessaire à la photosynthèse est consommé à partir de diverses sources, telles que la respiration des poissons, les processus de décomposition organique et les sels carbonatés dissous dans l’eau (KH), le tout dans un équilibre délicat et complexe, inexorablement régi et conditionné par le pH : À faible pH, le bicarbonate (HCO3) et le carbonate (CO3) se transforment enCO2. À pH neutre, la majeure partie duCO2 se transforme en bicarbonate (HCO3), tandis que le carbonate (CO3) prédomine à pH élevé. Ainsi, en ajustant la valeur du pH, on peut contrôler la quantité deCO2 disponible, indispensable au développement des plantes aquatiques.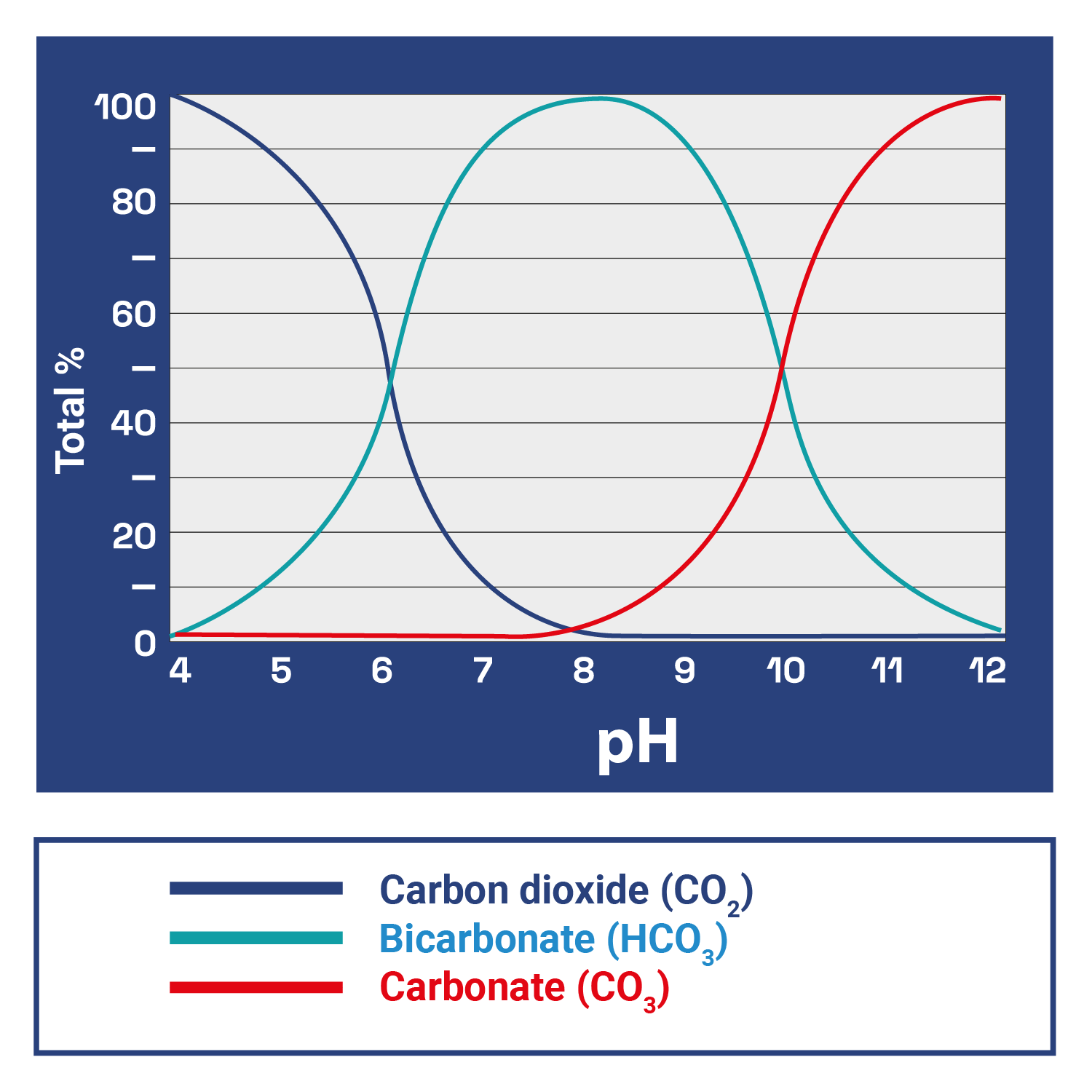
“L’eau de mer a un pH stable qui ne varie guère par rapport à 8,2. Cela signifie que les organismes vivant dans ces milieux n’ont pas développé une grande résistance aux variations de cette valeur”.
L’importance du pH dans notre aquarium marin.
La chimie de l’eau de mer est généralement beaucoup plus complexe et riche en minéraux que celle des rivières ou des lacs d’eau douce. Lorsque les minéraux sont en parfait équilibre dans un aquarium marin, le pH se situe entre 8,0 et 8,3. Cependant, en raison de l’action métabolique des poissons, des coraux et d’autres organismes, le pH d’un aquarium est modifié par la quantité, le type et la proportion de sels de carbonate dissous qui forment le KH (sels de carbonate, bicarbonate et borate). En effet, ces carbonates ont tendance à précipiter avec le calcium dissous (Ca+) pour former du carbonate de calcium (CaCO₃), mais ils peuvent également précipiter avec le magnésium (Mg) pour former du carbonate de magnésium (MgCO₃). Ces réactions se produisent lorsqu’il y a un excès ou une carence de l’un de ces sels, provoquant une chaîne de précipitations qui modifie le pH de l’eau.“Presque tous les organismes marins ont besoin de se développer dans un pH supérieur à 7,8 pour construire leur squelette, leurs épines, leurs spicules, leurs coquilles et d’autres structures”.En dessous de cette valeur, le CaCO₃ réagit avec l’eau et se dissout, ce qui a des conséquences graves pour presque tous les organismes marins. Dans les aquariums récifaux, nous maintenons souvent de nombreux organismes ayant une demande particulièrement élevée en calcium pour construire leur squelette ou leur coquille, tels que les coraux du genre Acropora spp. ou les mollusques du genre Tridacna spp. Ces espèces doivent également rester dans un gradient de pH très étroit et stable entre 8,20 et 8,30, faute de quoi elles commencent à perdre leur capacité à fixer le carbonate de calcium et à se développer. Bien que le pH approprié de l’eau de mer soit encore plus critique que celui de l’eau douce, nous avons un grand avantage : l’état alcalin de l’eau de mer permet auCO2 d’y pénétrer lorsqu’il est aéré à la surface, ce qui contribue à équilibrer le pH si le KH est à une valeur d’au moins 7° dKH (2,5 meq/l).
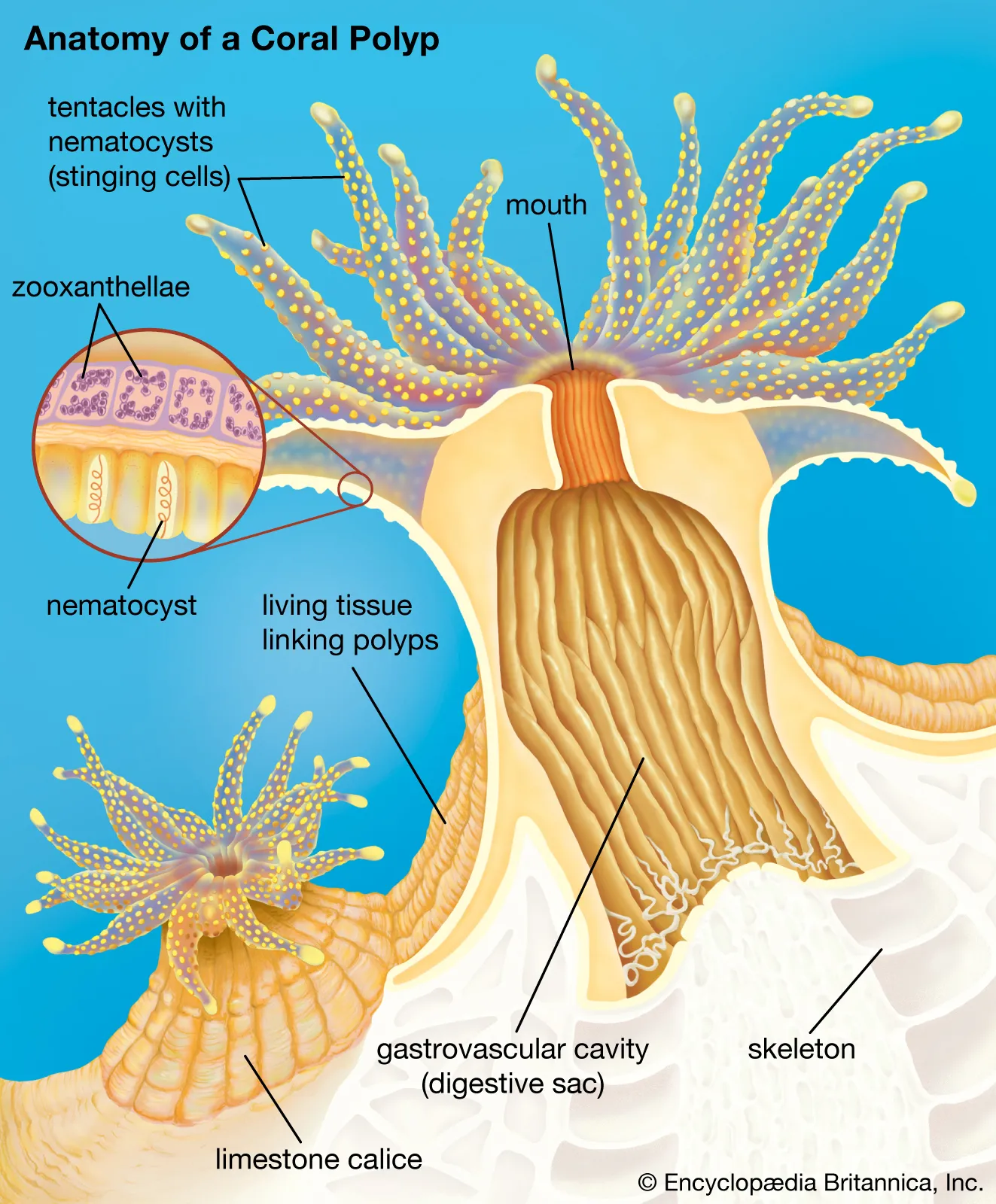
Le pH approprié pour les poissons d’eau douce et d’eau de mer.



D’accord, le pH est important. Mais comment le mesurer ?
Maintenant que nous comprenons mieux l’importance du pH dans notre aquarium et son influence décisive sur les organismes aquatiques, il est temps de s’attaquer à la partie la plus facile : le mesurer. Le marché actuel nous offre différentes méthodes de mesure du pH, toutes très faciles et rapides à utiliser. Analysons les avantages et les inconvénients qu’elles présentent pour vous aider à choisir celle qui vous convient le mieux. Méthodes colorimétriques : Cette méthode consiste à obtenir une couleur sur un liquide ou une bande de papier qui sera ensuite comparée à un étalon. En trouvant la couleur qui correspond le mieux à l’échantillon, nous obtenons notre mesure. Les deux méthodes les plus courantes sont les bandelettes réactives (comme le papier tournesol) et les kits d’indicateurs liquides. Les bandelettes présentent l’inconvénient d’une faible précision et d’une expiration rapide, ce qui réduit encore la précision. En revanche, les indicateurs liquides sont beaucoup plus pratiques et rapides. Il suffit de dissoudre quelques gouttes dans une certaine quantité d’eau dans un tube à essai et de comparer la couleur obtenue avec une charte colorimétrique. En quelques secondes, on connaît le résultat. Il est important d’acquérir un test de bonne qualité, proposé par une marque fiable et reconnue comme les tests pH AZOO.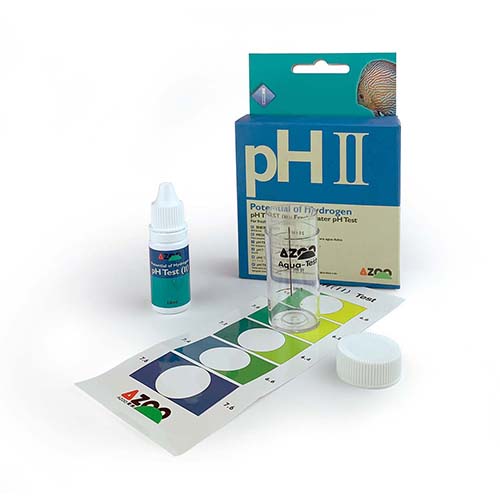

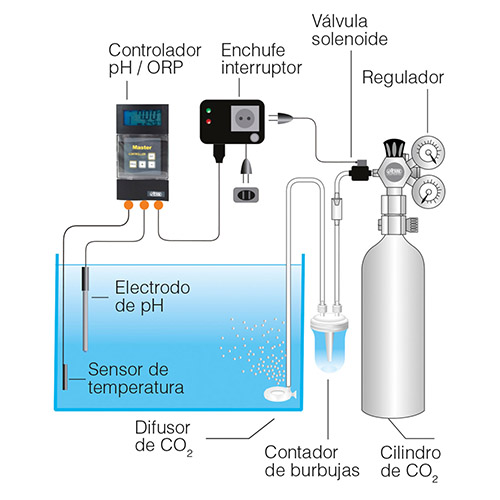
D’accord, il est très facile de mesurer le pH. Maintenant, comment puis-je le contrôler et le stabiliser dans l’aquarium ?
Si vous êtes arrivé jusqu’ici dans votre lecture, félicitations. Vous êtes prêt à contrôler le pH de votre aquarium. Pour contrôler le pH, le mieux est de commencer par le mesurer. Ensuite, nous ajouterons un conditionneur de pH approprié et sûr à l’eau pour le corriger facilement. Pour ce faire, le marché nous offre deux options : les conditionneurs de pH pour augmenter ou diminuer le pH et les tampons. Méthode des conditionneurs de type tampon. (Le concept “Buffer” est un terme anglo-saxon pour le concept chimique de “tampon” ou “buffering”). Ces additifs visent à donner à l’eau de l’aquarium un effet “tampon”, de sorte que le pH reste très stable à une valeur déterminée. Pour ce faire, ils modifient le facteur pKa de l’eau (le pKa est une mesure de la force de l’acidité). Cette méthode consiste à appliquer une formule qui combine le même sel sous ses formes acide et alcaline. En les combinant dans la bonne proportion, le fabricant obtient le facteur pKa qui stabilisera le pH là où nous le souhaitons. La technique du tampon est extrêmement simple, car non seulement nous obtenons le pH souhaité, mais nous le maintenons à cette valeur pendant plusieurs semaines. Une fois prédissous dans un peu d’eau, nous pouvons l’ajouter à l’eau que nous préparons pour un changement partiel ou directement dans l’aquarium. Tout cela sans courir le risque de surdoser l’additif. L’aspect le plus intéressant de ces “tampons” (et que peu d’amateurs connaissent) est la possibilité de les combiner pour obtenir et stabiliser la valeur de pH souhaitée dans chaque situation. L’autre méthode alternative est un peu plus avancée. Si nous voulons abaisser le pH, nous pouvons utiliser un conditionneur à base d’une combinaison de sels acides. Ce composé réagira avec les sels de carbonate (KH) et produira de l’acide carbonique (H₂CO₃), ce qui entraînera une diminution du pH. Il faut donc veiller à ne pas surdoser cet additif et à ne pas trop abaisser le pH. De nombreux fabricants, conscients de l’importance du pH dans notre aquarium, ont développé diverses solutions pour contrôler cet aspect. Certains amateurs avertis utilisent des acides très puissants à base de phosphore ou de soufre pour abaisser le pH, mais il s’agit d’une méthode de surdosage beaucoup plus agressive et risquée. En outre, ces acides sont extrêmement agressifs au contact de la peau et des yeux, et peuvent provoquer de graves brûlures chimiques. Une protection personnelle est nécessaire pour leur utilisation, ainsi qu’une expérience et des connaissances préalables pour les manipuler si l’on ne veut pas causer d’accident à soi-même ou à son aquarium. D’autre part, il est facile de provoquer des épidémies d’algues avec ces composés en raison du déséquilibre des nutriments qu’ils peuvent provoquer. Si notre pH est trop bas, il est très probable que la cause soit une alcalinité (KH) très faible. La méthode la plus fiable consiste une fois de plus à éviter les “remèdes maison”. Dans ce cas, nous vous recommandons d’ajouter une solution équilibrée de sels qui augmentent la dureté carbonatée de manière stable et contrôlable avec un conditionneur comme AZOO Plus Aquaguard.Conclusions :
A partir de cet article, nous pouvons souligner les points clés suivants pour comprendre l’importance du pH dans notre aquarium :
- Le pH indique l’acidité ou l’alcalinité de l’eau, en fonction de la concentration d’ions hydrogène chargés positivement dans une solution. Pour le mesurer, on utilise une échelle où le minimum est “0” comme acide, “7” est considéré comme neutre, et le maximum alcalin est “14”.
- Le pH est une valeur logarithmique et non linéaire, c’est pourquoi, lorsque nous le mesurons, nous devons être aussi précis et exacts que nos moyens le permettent.
- Le pH est certainement le paramètre le plus important de l’aquarium, avec le taux d’oxygène dissous et la température, car il affecte directement le métabolisme des organismes aquatiques à court terme.
- Le pH affecte directement la toxicité de l’ammoniac, il est donc beaucoup plus sûr de rester dans un pH légèrement acide en présence de ce composé azoté.
- Tous les organismes aquatiques n’ont pas la même tolérance aux variations de pH. Il faut savoir à quel gradient maximum et minimum ils sont adaptés afin d’éviter de les dépasser. A l’intérieur de leur propre gradient, le métabolisme des organismes souffre plus des changements brusques de pH que de rester à un extrême. Il faut donc leur offrir un temps d’acclimatation suffisant. À titre de référence, il est conseillé d’augmenter ou de diminuer d’un demi-point de pH toutes les 24 heures. (F. Castelló Orvay, 1993)
- Il est préférable de mesurer, contrôler et stabiliser le pH plutôt que de se demander si les symptômes d’un poisson ou d’un corail sont dus à une acidose ou à une alcalose. Vous n’êtes pas d’accord ?
- La méthode la plus pratique et la plus économique pour mesurer le pH est d’utiliser un kit de mesure réactif. Les stylos pH électroniques sont fortement recommandés malgré leur prix plus élevé. Ils coûtent probablement moins cher que les poissons que nous élevons.
- Le moyen le plus sûr et le plus pratique de contrôler et de stabiliser le pH de l’aquarium est d’utiliser des conditionneurs commerciaux de haute qualité. Nous pouvons modifier directement le pH de l’aquarium, en évitant de provoquer des changements trop brusques, mais la meilleure façon est de préparer la chimie de l’eau avant d’effectuer un changement partiel.



