“A maioria dos aquariofilistas já leu ou ouviu falar da importância do pH no nosso aquário. No entanto, muitos de nós não compreendem bem este conceito ou o seu papel fundamental na saúde dos organismos aquáticos”.
Por esta razão, hoje vamos abordar este aspeto tão familiar mas tão mal compreendido da qualidade da água, mas acima de tudo, o verdadeiro papel que desempenha no nosso aquário. Estás pronto?
O que é o pH?

Onde é que obtemos esses valores para determinar o pH?
É aqui que a explicação se torna um pouco complicada. Quando falamos de pH, estamos a referir-nos à concentração de iões de hidrogénio com carga positiva numa solução, chamados iões de hidrónio. A fórmula matemática para calcular o pH é o logaritmo negativo de base 10 da atividade do ião hidrogénio. pH = -log10 [aH+]. Por outras palavras, uma substância será tanto mais ácida quanto maior for a sua atividade de hidrogénio de carga positiva. Inversamente, quando a atividade é menor, a substância é mais alcalina.
Porque é que é importante saberes que o valor do pH é uma expressão logarítmica?
Estamos muito familiarizados com a medição da temperatura da água utilizando a escala Celsius, onde, por exemplo, um valor de 10°C é duas vezes mais frio do que 20°C, uma vez que estes valores formam uma escala linear ou geométrica. No entanto, se olharmos para a fórmula do pH, veremos que estamos a lidar com uma expressão logarítmica. Isto significa que um valor de pH de 7,0 é neutro, mas ao mesmo tempo é dez vezes mais ácido do que um pH de 8,0, cem vezes mais ácido do que um pH de 9,0, e mil vezes mais ácido do que um pH de 10,0, e assim por diante.
“É importante manter o pH mais ou menos neutro, entre 6 e 8.”
E é claro que, na realidade, esta frase se refere a um gradiente com uma diferença até 100 vezes maior, demasiado imprecisa para os requisitos de qualidade da água em qualquer aquário. É como se dissesses:“É importante manter a água quente, entre 0 °C e 100 °C.”
“Devemos prestar atenção ao valor do pH do nosso aquário, medindo-o com toda a precisão e exatidão de que dispomos”.
O pH é um parâmetro físico.
Parâmetros químicos como a dureza (GH), os nitritos (NO2), os fosfatos (PO₄³-) ou o oxigénio dissolvido (O2) indicam a concentração de vários elementos ou compostos dissolvidos na água, que são muito úteis para determinar a qualidade da água. Em contrapartida, os parâmetros físicos como o pH, a temperatura, a densidade, a condutividade ou o potencial REDOX indicam o estado da água; se é ácida ou alcalina, oxidante ou redutora, quente ou fria, densa ou fluida, condutora ou isolante, etc. Os parâmetros físicos também se caracterizam por influenciar todos os outros parâmetros, sejam eles físicos ou químicos, e o pH não é exceção. Vejamos um dos exemplos mais proeminentes para compreenderes a importância do pH no nosso aquário:Influência na toxicidade do amoníaco/amónio na água.
O amónio presente na água de um aquário surge como resultado das excreções dos peixes e de outros resíduos orgânicos, como o tecido vegetal em decomposição. A presença de amónio inicia o processo bacteriano conhecido como “Ciclo do Azoto”. Quando o azoto (N) está presente na água (H2O), pode combinar-se com o hidrogénio (H+ / OH-), formando amoníaco (NH3) ou amónio (NH4+), dependendo do pH do aquário. Se o valor do pH for ácido, o azoto combina-se para formar NH4+, enquanto que se for alcalino, forma NH3. Isto é fundamental para determinar a toxicidade da água porque o amoníaco é 200 a 300 vezes mais tóxico do que o amónio. (Hinton DE, Laurén DJ, 1992)
“Durante o ciclo, é preferível que os aquários mantenham um pH inferior a 7,0, uma vez que os níveis de amoníaco serão elevados durante os primeiros dias”.A exceção é para os aquários cujos habitantes requerem valores de pH alcalinos, como os de água salgada, água salobra ou ciclídeos africanos. Vamos dar uma olhadela:
A importância do pH para os organismos aquáticos.
Espículas, talos, esqueletos, conchas, espinhos e dentes.
Com raras excepções, como os tunicados (ascídias), a maioria dos organismos aquáticos precisa de produzir carbonato de cálcio (CaCO3) para construir os seus tecidos rígidos, essenciais para a sua defesa e várias funções vitais. No entanto, este mineral reage dissolvendo-se na água quando o pH desce abaixo de 7,8. Isto impede a criação de novos tecidos e enfraquece seriamente os tecidos já formados. Esta síndrome de descalcificação é especialmente crítica nos organismos adaptados a viver em águas alcalinas.Metabolismo e saúde dos peixes.
Sabemos que nem todos os peixes têm a mesma tolerância às alterações de pH, embora devamos ter em mente que se nos desviarmos deste intervalo, os problemas de saúde não tardarão a aparecer. Vejamos porquê: A médio prazo, um pH demasiado ácido provoca problemas de depósitos de cálcio nos rins (nefrocalcinose) e descalcificação nos tecidos duros. Afecta também o crescimento devido a problemas de apetite e de absorção dos nutrientes.“Os efeitos mais imediatos de um valor de pH inadequado nos peixes são a redução da sua eficiência respiratória e da capacidade do seu sistema osmorregulador”.
A síndrome da acidose.
A curto prazo, um pH demasiado baixo provoca uma diminuição drástica da capacidade da hemoglobina do sangue para absorver oxigénio (efeito de Bohr, Wedemeyer, 1996). Isto leva a um excesso de CO2 no sangue (hipercapnia) com a consequente diminuição do pH (o sangue dos peixes tem uma variação entre 7,7 e 8,0). Como resultado, os peixes afectados podem tornar-se letárgicos, arfar à superfície da água e apresentar uma respiração acelerada.

O pH num aquário com plantas.
Durante o dia, as plantas aquáticas absorvem dióxido de carbono (CO2) e libertam oxigénio (O2) durante a fotossíntese, aumentando o pH. Inversamente, à noite, invertem este processo, respirando O2 e libertandoCO2, que reage com a água para formar ácido carbónico (H₂CO₃), baixando o pH. Num ambiente confinado como um aquário, o metabolismo das plantas aquáticas modificará severamente o pH do aquário em ciclos de 12 horas se não houver minerais tampão suficientes como os carbonatos (KH). A importância do pH no nosso aquário plantado é ainda mais crítica se pretendemos ter sucesso no nosso projeto. O carbono necessário para a fotossíntese é consumido a partir de várias fontes, como a respiração dos peixes, os processos de decomposição orgânica e os sais de carbonato dissolvidos na água (KH), tudo num equilíbrio delicado e complexo, inexoravelmente regido e condicionado pelo pH: Em pH baixo, o bicarbonato (HCO3) e o carbonato (CO3) convertem-se emCO2. Em pH neutro, a maior parte doCO2 converte-se em bicarbonato (HCO3), enquanto o carbonato (CO3) predomina em pH elevado. Assim, ao ajustar o valor do pH, podemos controlar a quantidade deCO2 disponível, que é essencial para o desenvolvimento das plantas aquáticas.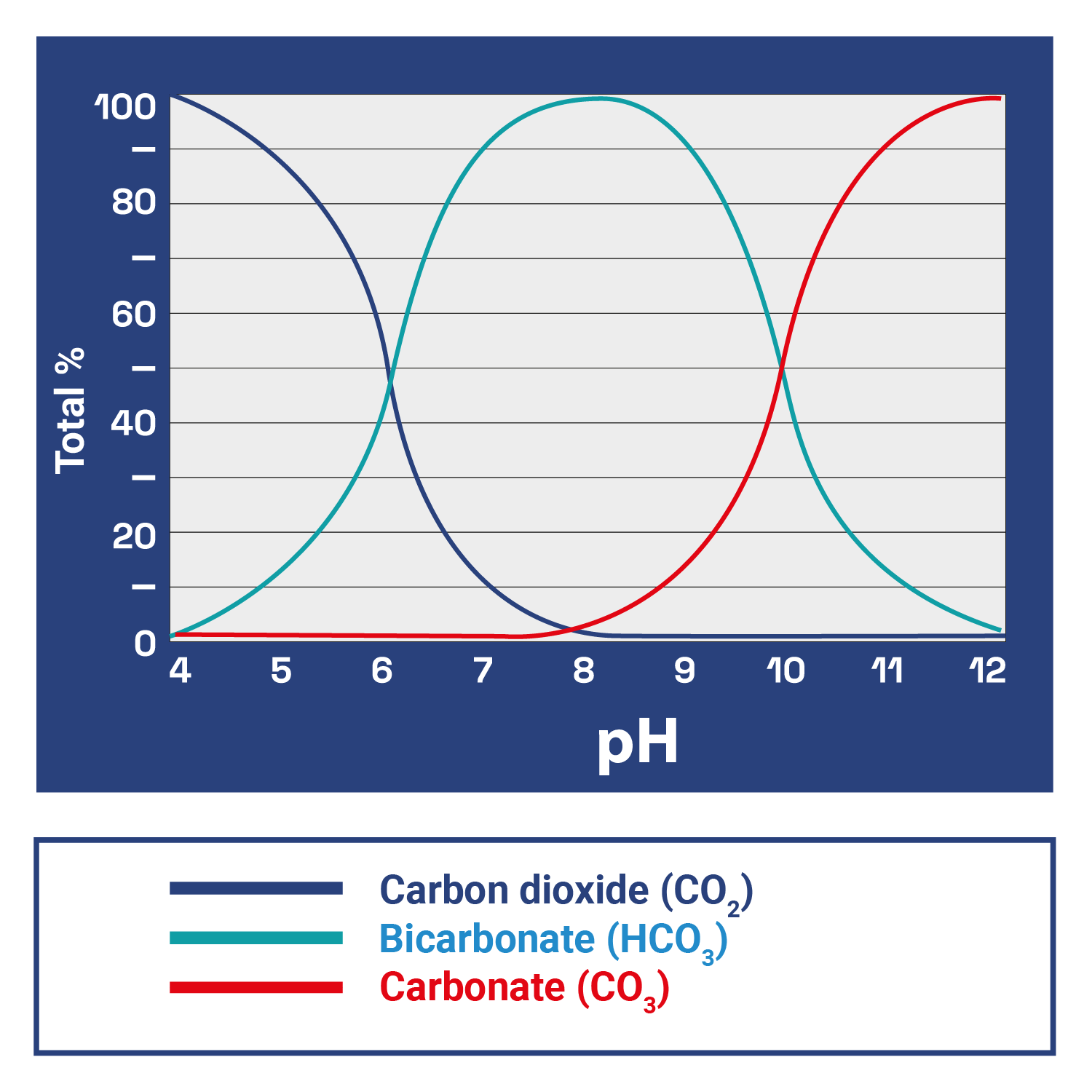
“A água do mar tem um pH estável que dificilmente varia de 8,2. Isto significa que os organismos que vivem nestes ambientes não desenvolveram muita resistência às variações deste valor”.
A importância do pH no teu aquário marinho.
A química da água do mar é normalmente muito mais complexa e rica em minerais do que a dos rios ou lagos de água doce. Quando os minerais estão em perfeito equilíbrio num aquário marinho, o pH varia entre 8,0 e 8,3. No entanto, devido à ação metabólica dos peixes, corais e outros organismos, o pH de um aquário é alterado pela quantidade, tipo e proporção de sais de carbonato dissolvidos que formam o KH (sais de carbonato, bicarbonato e borato). A razão é que estes carbonatos tendem a precipitar com o cálcio dissolvido (Ca+) para formar carbonato de cálcio (CaCO₃), mas também podem precipitar com o magnésio (Mg) para formar carbonato de magnésio (MgCO₃). Estas reacções ocorrem quando há excesso ou deficiência de qualquer um destes sais, provocando uma cadeia de precipitações que alteram o pH da água.“Quase todos os organismos marinhos precisam de se desenvolver num pH superior a 7,8 para construir o seu esqueleto, espinhos, espículas, conchas e outras estruturas”.Abaixo deste valor, o CaCO₃ reage com a água, dissolvendo-se, o que tem consequências graves para quase todos os organismos marinhos. Nos aquários de recife, é frequente mantermos muitos organismos com uma necessidade particularmente elevada de cálcio para construir os seus esqueletos ou conchas, como os corais do género Acropora spp. ou moluscos do género Tridacna spp. Estas espécies também necessitam de permanecer num gradiente de pH muito estreito e estável entre 8,20 – 8,30, caso contrário começam a perder a sua capacidade de fixar carbonato de cálcio e de se desenvolver. Apesar de o pH adequado na água salgada ser ainda mais crítico do que na água doce, temos uma grande vantagem: o estado alcalino da água do mar permite queo CO2 penetre nela quando arejado à superfície, ajudando a equilibrar o pH se o KH tiver um valor de pelo menos 7° dKH (2,5 meq/l).
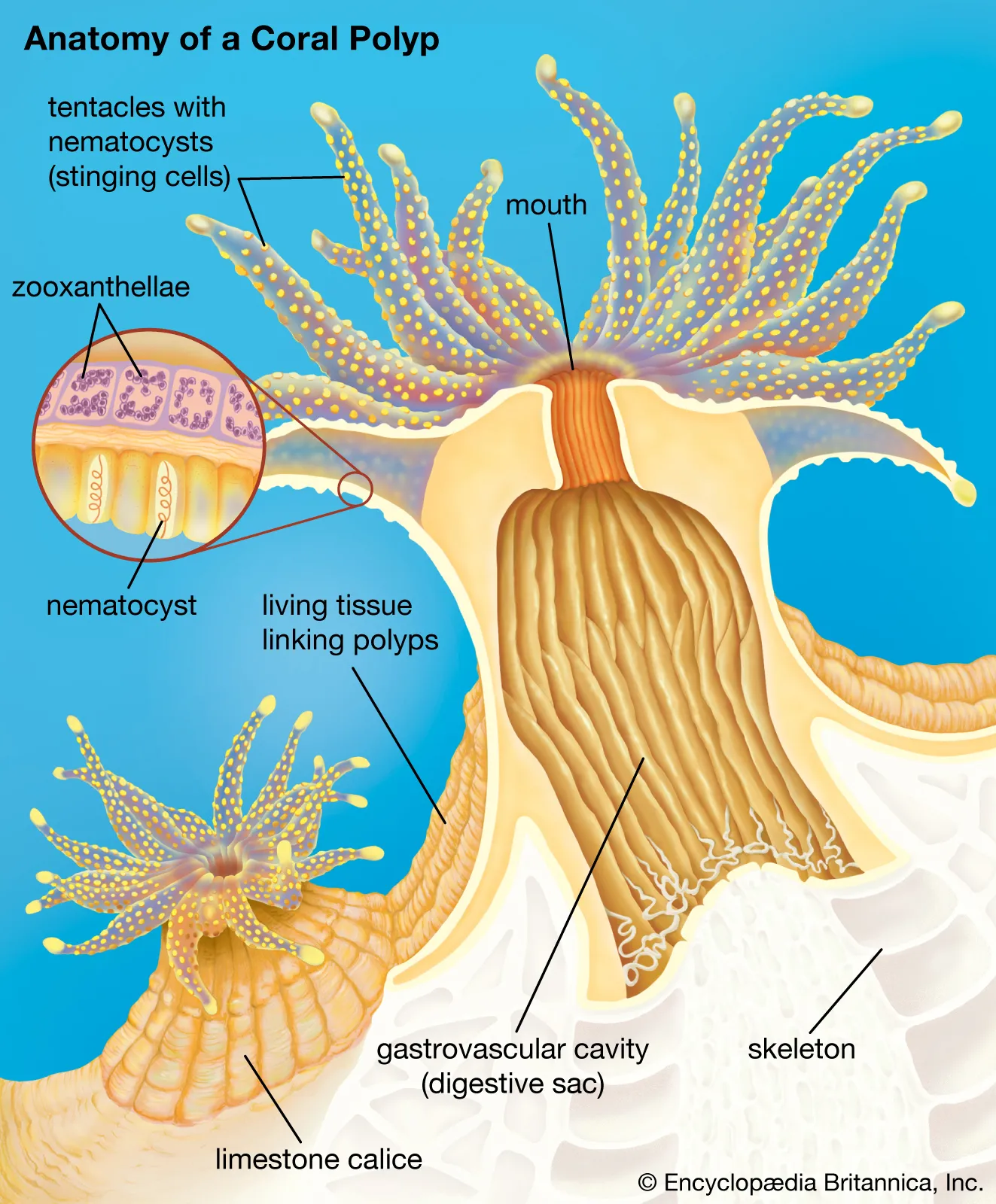
O pH adequado para peixes de água doce e de água salgada.



Muito bem, o pH é importante. Mas, como é que o medimos?
Agora que já compreendemos melhor a importância do pH no nosso aquário e a sua influência decisiva nos organismos aquáticos, está na altura de abordar a parte mais fácil: medi-lo. O mercado atual oferece-nos vários métodos de medição do pH, todos eles muito fáceis e rápidos de utilizar. Vamos analisar as vantagens e desvantagens que apresentam para te ajudar a escolher o mais adequado. Métodos colorimétricos: Este método envolve a obtenção de uma cor num líquido ou numa tira de papel para depois ser comparada com um padrão. Ao encontrar a cor mais próxima da amostra, obtemos a nossa medição. Os dois métodos mais comuns são as tiras de teste de medição (como o papel de tornassol) e os kits de indicadores líquidos. As tiras de teste têm a desvantagem da baixa precisão e da expiração rápida, o que reduz ainda mais a exatidão. Em contrapartida, os indicadores líquidos são muito mais práticos e rápidos. Basta dissolver algumas gotas numa certa quantidade de água num tubo de ensaio e comparar a cor resultante com uma tabela colorimétrica. Em poucos segundos, saberás o resultado. É importante adquirires um teste de boa qualidade, oferecido por uma marca de confiança e reconhecida, como é o caso dos testes de pH AZOO.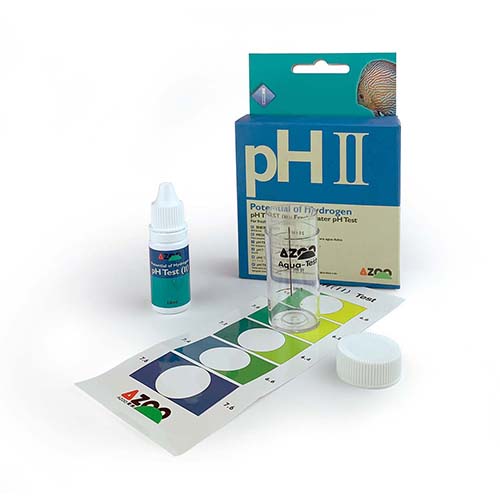

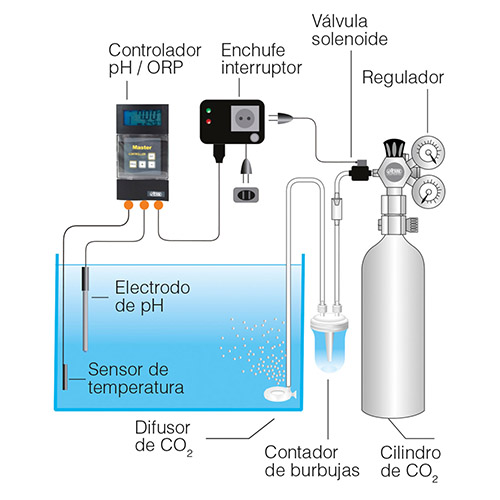
Ok, medir o pH é muito fácil. Agora, como é que o posso controlar e estabilizar no aquário?
Se chegaste até aqui na tua leitura, parabéns. Estás mais do que pronto para controlar o pH do teu aquário. Para controlar o pH, a melhor maneira é começar por medi-lo. Em seguida, adicionaremos à água um condicionador de pH adequado e seguro para corrigi-lo facilmente. Para este efeito, o mercado oferece-nos duas opções: os condicionadores de pH para aumentar ou diminuir o pH e os tampões. Método dos amaciadores do tipo tampão. (O conceito “Buffer” é um termo anglo-saxónico para o conceito químico de “buffer” ou “buffering”). Estes aditivos têm como objetivo dar à água do aquário um efeito “tampão”, para que o pH se mantenha muito estável num determinado valor. Para isso, alteram o fator pKa da água (o pKa é uma medida do grau de acidez). Este método consiste em aplicar uma fórmula que combina o mesmo sal nas suas formas ácida e alcalina. Combinando-as na proporção correta, o fabricante obtém o fator pKa que estabilizará o pH onde o desejamos. A técnica do tampão é extremamente simples, pois não só obtemos o pH desejado, como também o mantemos nesse valor durante várias semanas. Uma vez pré-dissolvido num pouco de água, podemos adicioná-lo à água que estamos a preparar para uma mudança parcial ou diretamente no aquário. Tudo isto sem correr um grande risco de sobredosagem do aditivo. O aspeto mais interessante destes “tampões” (e que poucos amadores conhecem) é a possibilidade de os combinar para obter e estabilizar o valor de pH que pretendemos em cada situação. O outro método alternativo é um pouco mais avançado. Se quiseres baixar o pH, podes usar um condicionador à base de uma combinação de sais ácidos. Este composto irá reagir com sais de carbonato (KH), resultando em ácido carbónico (H₂CO₃), o que fará com que o pH diminua. Só precisamos de ter cuidado para não exagerar na dose deste aditivo e baixar demasiado o pH. Muitos fabricantes, conscientes da importância do pH no nosso aquário, desenvolveram várias soluções para controlar este aspeto. Alguns aquariofilistas avançados usam ácidos muito fortes à base de fósforo ou enxofre para baixar o pH, mas é um método muito mais agressivo e arriscado de sobredosagem. Além disso, estes ácidos são extremamente agressivos quando em contacto com a pele e os olhos, podendo causar queimaduras químicas graves. É necessária proteção pessoal para a sua utilização, bem como experiência e conhecimentos prévios no seu manuseamento, se não quisermos causar um acidente a nós próprios ou ao nosso aquário. Por outro lado, é fácil causar surtos de algas com estes compostos devido ao desequilíbrio de nutrientes que podem causar. Se o nosso pH for demasiado baixo, é muito provável que a causa seja uma alcalinidade (KH) muito baixa. O método mais fiável é, mais uma vez, evitar os “remédios caseiros”. Neste caso, recomendamos que adiciones uma solução equilibrada de sais que aumentem a dureza carbonatada de forma estável e controlável com um condicionador como o AZOO Plus Aquaguard.Conclusões:
A partir deste artigo, podemos destacar os seguintes pontos-chave para compreenderes a importância do pH no nosso aquário:
- O pH indica a acidez ou alcalinidade da água, com base na concentração de iões de hidrogénio com carga positiva numa solução. Para o medir, utilizamos uma escala em que o mínimo é “0” como ácido, “7” é considerado neutro e o valor alcalino máximo é “14”.
- O pH é um valor logarítmico e não linear, pelo que, ao medi-lo, devemos ser tão precisos e exactos quanto os nossos meios o permitam.
- O pH é definitivamente o parâmetro mais importante do aquário, juntamente com a taxa de oxigénio dissolvido e a temperatura, pois afecta diretamente o metabolismo dos organismos aquáticos a curto prazo.
- O pH afecta diretamente a toxicidade do amoníaco, pelo que é muito mais seguro manter um pH ligeiramente ácido na presença deste composto de azoto.
- Nem todos os organismos aquáticos têm a mesma tolerância às alterações de pH. É preciso descobrir qual é o gradiente máximo e mínimo a que estão adaptados para evitar ultrapassá-lo. Dentro do seu próprio gradiente, o metabolismo dos organismos sofre mais com as mudanças bruscas de pH do que com a permanência num extremo. Por isso, é preciso dar tempo suficiente para a sua aclimatação. Como referência, é aconselhável aumentar ou diminuir meio ponto de pH a cada 24 horas. (F. Castelló Orvay, 1993)
- É preferível medir, controlar e estabilizar o pH em vez de te perguntares se os sintomas de um peixe ou coral se devem a acidose ou alcalose. Não estás de acordo?
- O método mais prático e económico para medir o pH é utilizar um kit de medição reactiva. As canetas electrónicas de pH são altamente recomendadas, apesar do seu preço mais elevado. Provavelmente custam menos dinheiro do que os peixes que mantemos.
- A maneira mais segura e prática de controlar e estabilizar o pH do aquário é utilizar condicionadores comerciais de alta qualidade. Podemos modificar diretamente o pH do aquário, evitando provocar alterações muito bruscas, mas a melhor maneira é preparar a química da água antes de efetuar uma mudança parcial.



