“La mayoría de los aficionados han leído o escuchado alguna vez lo importante que es el pH en nuestro acuario. Sin embargo, muchos de nosotros no acabamos de entender este concepto ni su papel fundamental en la salud de los organismos acuáticos”.
Por eso, hoy vamos a abordar este aspecto tan conocido y a la vez tan incomprendido de la calidad del agua, pero sobre todo, el verdadero papel que desempeña en nuestro acuario. ¿Preparados?
¿Qué es el pH?

¿De dónde obtenemos esos valores para determinar el pH?
Aquí es donde la explicación se complica un poco. Cuando hablamos de pH, en realidad nos referimos a la concentración de iones de hidrógeno cargados positivamente en una solución, llamados iones hidronio. La fórmula matemática para calcular el pH es el logaritmo negativo de base 10 de la actividad del ion hidrógeno. pH = -log10 [aH+]. En otras palabras, una sustancia será más ácida cuanto mayor sea su actividad de hidrógeno cargado positivamente. A la inversa, cuando haya menos actividad, la sustancia será más alcalina.
¿Por qué es importante saber que el valor del pH es una expresión logarítmica?
Estamos muy familiarizados con la medición de la temperatura del agua mediante la escala Celsius, en la que, por ejemplo, un valor de 10 °C es el doble de frío que 20 °C, ya que estos valores forman una escala lineal o geométrica. Sin embargo, si nos fijamos en la fórmula del pH, veremos que se trata de una expresión logarítmica. Esto implica que un valor de pH de 7,0 es neutro, pero al mismo tiempo es diez veces más ácido que un pH de 8,0, cien veces más ácido que un pH de 9,0 y mil veces más ácido que un pH de 10,0, y así sucesivamente.
“Es importante mantener el pH más o menos neutro, entre 6 y 8”.
Y claro, en realidad, esa frase se refiere a un gradiente con una diferencia de hasta 100 veces mayor, demasiado impreciso para los requisitos de calidad del agua en cualquier acuario. Es como decir“Es importante mantener el agua caliente, entre 0 °C y 100 °C”.
“Debemos prestar atención al valor de pH de nuestro acuario, midiéndolo con toda la precisión y exactitud de que dispongamos”.
El pH es un parámetro físico.
Los parámetros químicos como la dureza (GH), el nitrito (NO2), el fosfato (PO₄³-) o el oxígeno disuelto (O2) indican la concentración de diversos elementos o compuestos disueltos en el agua, que son muy útiles para determinar la calidad del agua. En cambio, los parámetros físicos como el pH, la temperatura, la densidad, la conductividad o el potencial REDOX indican el estado del agua; si es ácida o alcalina, oxidante o reductora, caliente o fría, densa o fluida, conductora o aislante, etc. Los parámetros físicos también se caracterizan por influir en todos los demás parámetros, ya sean físicos o químicos, y el pH no es una excepción. Veamos uno de los ejemplos más destacados para comprender la importancia del pH en nuestro acuario:Influencia en la toxicidad del amoníaco/amonio en el agua.
El amonio presente en el agua de un acuario surge como resultado de las excreciones de los peces y otros residuos orgánicos, como el tejido vegetal en descomposición. La presencia de amonio inicia el proceso bacteriano conocido como “Ciclo del Nitrógeno”. Cuando el nitrógeno (N) está presente en el agua (H2O), puede combinarse con el hidrógeno (H+ / OH-) como amoníaco (NH3) o amonio (NH4+), dependiendo del pH del acuario. Si el pH es ácido, el nitrógeno se combina para formar NH4+, mientras que si es alcalino, forma NH3. Esto es fundamental para determinar la toxicidad del agua, porque el amoníaco es entre 200 y 300 veces más tóxico que el amonio. (Hinton DE, Laurén DJ, 1992)
“Durante el ciclado, es preferible que los acuarios mantengan un pH inferior a 7,0, ya que los niveles de amoníaco serán elevados durante los primeros días”.La excepción son los acuarios cuyos habitantes requieren valores de pH alcalinos, como los de agua salada, salobre o cíclidos africanos. Echemos un vistazo:
La importancia del pH en los organismos de la vida acuática.
Espículas, talos, esqueletos, conchas, espinas y dientes.
Salvo raras excepciones como los tunicados (ascidias), la mayoría de los organismos acuáticos necesitan producir carbonato cálcico (CaCO3) para construir sus tejidos rígidos, esenciales para su defensa y diversas funciones vitales. Sin embargo, este mineral reacciona disolviéndose en el agua cuando el pH desciende por debajo de 7,8. Esto dificulta la creación de nuevos tejidos y debilita gravemente los ya formados. Este síndrome de descalcificación es especialmente crítico en organismos adaptados a vivir en aguas alcalinas.Metabolismo y salud de los peces.
Sabemos que no todos los peces tienen la misma tolerancia a las alteraciones del pH, aunque debemos tener en cuenta que si nos desviamos de este intervalo, pronto aparecerán problemas de salud. Veamos por qué: A medio plazo, un pH demasiado ácido provoca problemas de depósitos de calcio en los riñones (nefrocalcinosis) y descalcificación en los tejidos duros. También afecta al crecimiento debido a problemas de apetito y absorción de nutrientes.“Los efectos más inmediatos de un valor de pH inadecuado en los peces son la reducción de su eficacia respiratoria y de la capacidad de su sistema osmorregulador”.
El síndrome de acidosis.
A corto plazo, un pH demasiado bajo provoca una disminución drástica de la capacidad de la hemoglobina de la sangre para absorber oxígeno (efecto Bohr, Wedemeyer, 1996). Esto provoca un exceso de CO2 en la sangre (hipercapnia) con la consiguiente disminución del pH (la sangre de los peces tiene un rango entre 7,7 y 8,0). Como resultado, el pez afectado puede volverse letárgico, jadear en la superficie del agua y mostrar una respiración acelerada.

El pH en un acuario plantado.
Durante el día, las plantas acuáticas absorben dióxido de carbono (CO2) y liberan oxígeno (O2) durante la fotosíntesis, elevando el pH. A la inversa, por la noche, invierten este proceso, respirando O2 y liberandoCO2, que reacciona con el agua para formar ácido carbónico (H₂CO₃), bajando el pH. En un entorno confinado como un acuario, el metabolismo de las plantas acuáticas modificará gravemente el pH del acuario en ciclos de 12 horas si no hay suficientes minerales amortiguadores como los carbonatos (KH). La importancia del pH en nuestro acuario plantado es aún más crítica si pretendemos tener éxito en nuestro proyecto. El carbono necesario para la fotosíntesis se consume de diversas fuentes, como la respiración de los peces, los procesos de descomposición orgánica y las sales carbonatadas disueltas en el agua (KH), todo ello en un delicado y complejo equilibrio, inexorablemente regido y condicionado por el pH: A pH bajo, el bicarbonato (HCO3) y el carbonato (CO3) se convierten enCO2. A pH neutro, la mayor parte delCO2 se convierte en bicarbonato (HCO3), mientras que a pH alto predomina el carbonato (CO3). Así, ajustando el valor del pH, podemos controlar la cantidad deCO2 disponible, que es esencial para el desarrollo de las plantas acuáticas.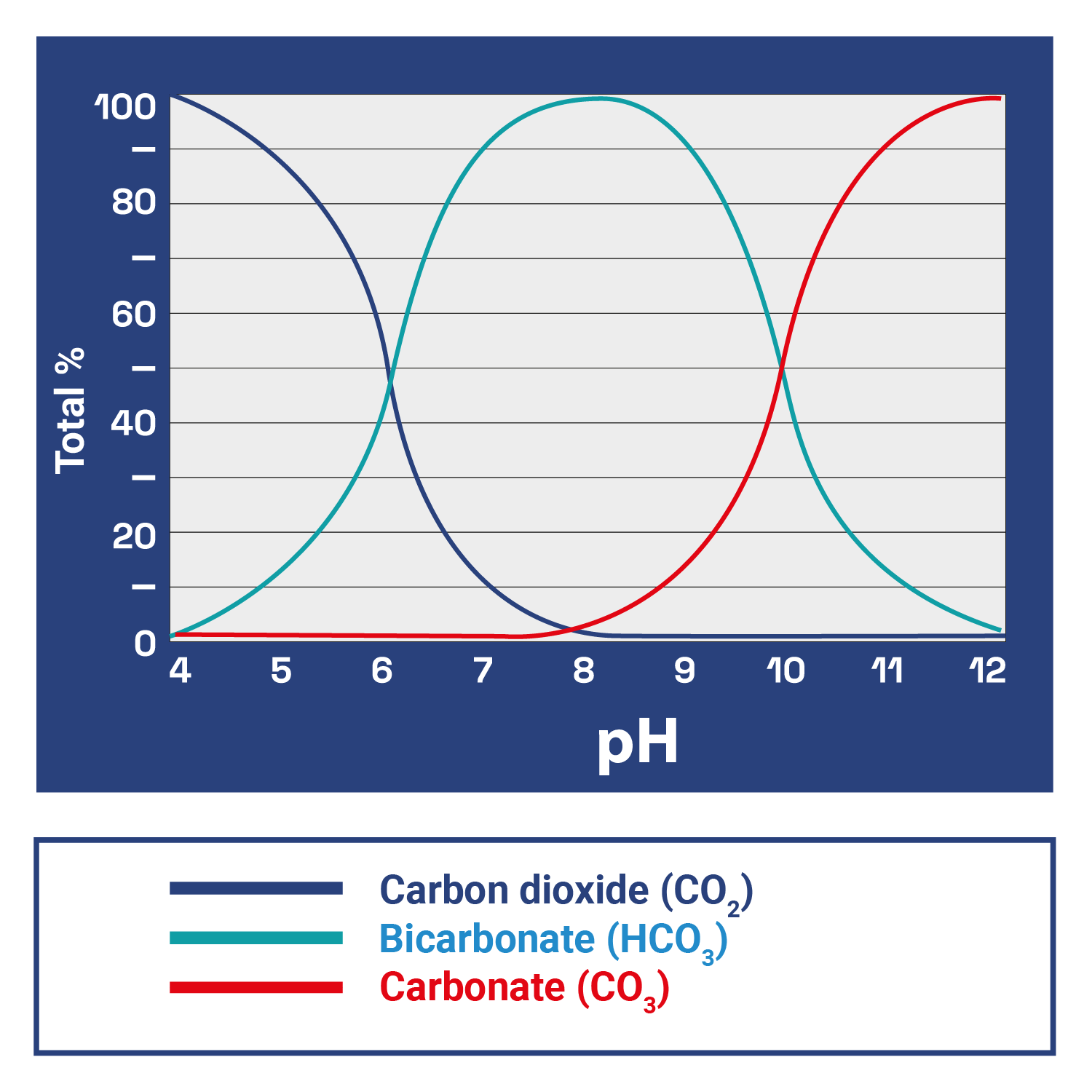
“El agua de mar tiene un pH estable que apenas varía de 8,2. Esto significa que los organismos que viven en estos entornos no han desarrollado mucha resistencia a las variaciones de este valor”.
La importancia del pH en nuestro acuario marino.
La química del agua de mar suele ser mucho más compleja y rica en minerales que la de los ríos o lagos de agua dulce. Cuando los minerales están en perfecto equilibrio en un acuario marino, el pH oscila entre 8,0 y 8,3. Sin embargo, debido a la acción metabólica de los peces, corales y otros organismos, el pH de un acuario se ve alterado por la cantidad, tipo y proporción de sales de carbonato disueltas que forman el KH (sales de carbonato, bicarbonato y borato). La razón es que estos carbonatos tienden a precipitar con el calcio disuelto (Ca+) para formar carbonato cálcico (CaCO₃), pero también pueden precipitar con el magnesio (Mg) para formar carbonato magnésico (MgCO₃). Estas reacciones se producen cuando hay un exceso o una carencia de alguna de estas sales, provocando una cadena de precipitaciones que alteran el pH del agua.“Casi todos los organismos marinos necesitan desarrollarse en un pH superior a 7,8 para construir su esqueleto, espinas, espículas, conchas y otras estructuras”.Por debajo de este valor, el CaCO₃ reacciona con el agua, disolviéndose, lo que tiene graves consecuencias para casi todos los organismos marinos. En los acuarios de arrecife, a menudo mantenemos muchos organismos con una demanda especialmente alta de calcio para construir sus esqueletos o conchas, como los corales del género Acropora spp. o moluscos del género Tridacna spp. Estas especies también necesitan permanecer en un gradiente de pH muy estrecho y estable, entre 8,20 y 8,30, o de lo contrario empiezan a perder su capacidad de fijar carbonato cálcico y desarrollarse. A pesar de que el pH adecuado en agua salada es aún más crítico que en agua dulce, tenemos una gran ventaja: la condición alcalina del agua de mar permite queel CO2 penetre en ella cuando se airea en la superficie, ayudando a equilibrar el pH si el KH está en un valor de al menos 7° dKH (2,5 meq/l).
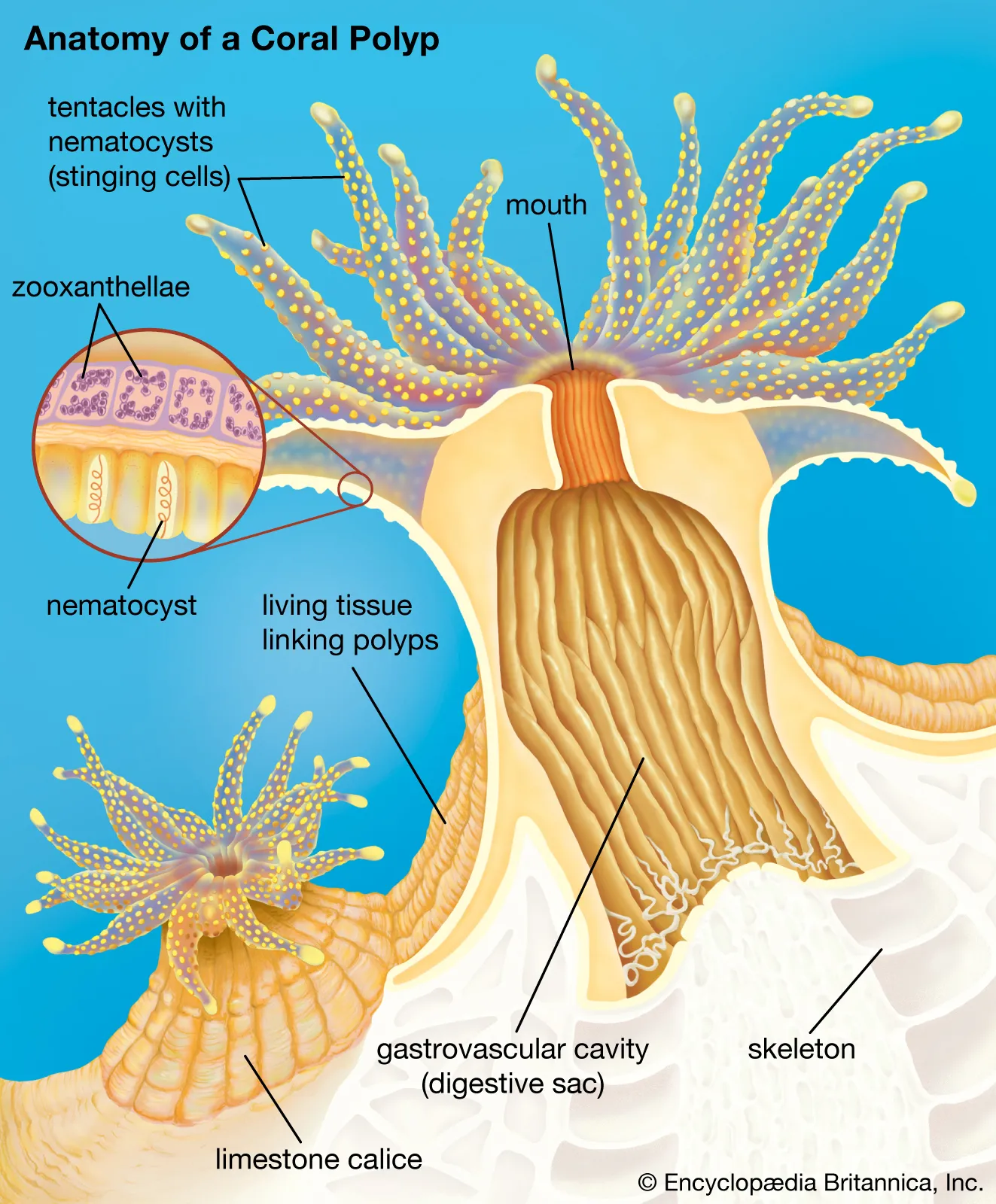
El pH adecuado para peces de agua dulce y salada.



De acuerdo, el pH es importante. Pero, ¿cómo lo medimos?
Ahora que conocemos mejor la importancia del pH en nuestro acuario y su influencia decisiva en los organismos acuáticos, es hora de abordar la parte más fácil: medirlo. El mercado actual nos ofrece varios métodos para medir el pH, todos ellos muy fáciles y rápidos de utilizar. Analicemos las ventajas e inconvenientes que presentan para ayudarte a elegir el más adecuado. Métodos colorimétricos: Este método consiste en obtener un color en una tira líquida o de papel para luego compararlo con un patrón. Encontrando la coincidencia de color más cercana con la muestra, obtenemos nuestra medida. Los dos métodos más habituales son las tiras reactivas de medición (como el papel tornasol) y los kits de indicadores líquidos. Las tiras reactivas tienen el inconveniente de su escasa precisión y rápida caducidad, lo que reduce aún más la exactitud. En cambio, los indicadores líquidos son mucho más prácticos y rápidos. Basta con disolver unas gotas en cierta cantidad de agua en un tubo de ensayo y comparar el color resultante con una tabla colorimétrica. En unos segundos, sabremos el resultado. Es importante adquirir un test de buena calidad, ofrecido por una marca de confianza y reconocida, como los tests de pH AZOO.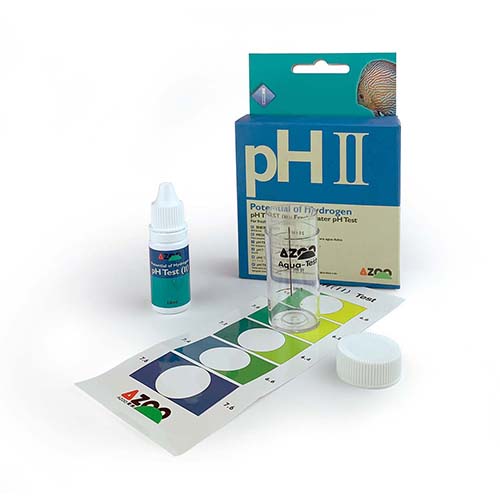

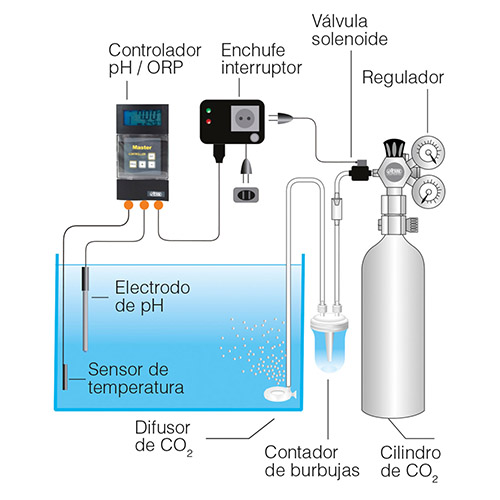
Vale, medir el pH es muy fácil. Ahora bien, ¿cómo puedo controlarlo y estabilizarlo en el acuario?
Si has llegado hasta aquí en tu lectura, enhorabuena. Estás más que preparado para tomar el control del pH de tu acuario. Para controlar el pH, lo mejor es empezar por medirlo. Después, añadiremos al agua un acondicionador del pH adecuado y seguro para corregirlo fácilmente. Para ello, el mercado nos ofrece dos opciones: acondicionadores de pH para subir o bajar el pH, y tampones. Método de los acondicionadores de tipo tampón. (El concepto “Buffer” es un término anglosajón que designa el concepto químico de “tampón” o “amortiguador”). Estos aditivos pretenden dar al agua del acuario un efecto “tampón”, de modo que el pH se mantenga muy estable en un valor determinado. Para conseguirlo, alteran el factor pKa del agua (el pKa es una medida de la fuerza de la acidez). Este método consiste en aplicar una fórmula que combina la misma sal en sus formas ácida y alcalina. Combinándolas en la proporción correcta, el fabricante obtiene el factor pKa que estabilizará el pH donde queremos. La técnica del tampón es extremadamente sencilla, ya que no sólo conseguimos el pH deseado, sino que lo mantenemos en ese valor durante varias semanas. Una vez predisuelto en un poco de agua, podemos añadirlo al agua que estamos preparando para un cambio parcial o directamente al acuario. Todo ello sin correr un gran riesgo de sobredosificar el aditivo. El aspecto más interesante de estos “tampones” (y que pocos aficionados conocen) es la posibilidad de combinarlos para obtener y estabilizar el valor de pH que deseemos en cada situación. El otro método alternativo es un poco más avanzado. Si queremos bajar el pH, podemos utilizar un acondicionador basado en una combinación de sales ácidas. Este compuesto reaccionará con las sales de carbonato (KH) dando lugar a ácido carbónico (H₂CO₃), que hará que disminuya el pH. Sólo hay que tener cuidado de no sobredosificar este aditivo y bajar demasiado el pH. Muchos fabricantes, conscientes de la importancia del pH en nuestro acuario, han desarrollado diversas soluciones para controlar este aspecto. Algunos aficionados avanzados utilizan ácidos muy fuertes a base de fósforo o azufre para bajar el pH, pero es un método mucho más agresivo y arriesgado de sobredosificar. Además, estos ácidos son extremadamente agresivos en contacto con la piel y los ojos, pudiendo causar quemaduras químicas graves. Es necesaria la protección personal para su uso, así como experiencia y conocimientos previos en su manipulación si no queremos causarnos un accidente a nosotros mismos o a nuestro acuario. Por otra parte, es fácil provocar brotes de algas con estos compuestos debido al desequilibrio de nutrientes que pueden causar. Si nuestro pH es demasiado bajo, es muy probable que la causa sea una alcalinidad (KH) muy baja. El método más fiable es, una vez más, evitar los “remedios caseros”. En este caso, recomendamos añadir una solución equilibrada de sales que aumenten la dureza de carbonatos de forma estable y controlable con un acondicionador como AZOO Plus Aquaguard.Conclusiones:
De este artículo, podemos destacar los siguientes puntos clave para comprender la importancia del pH en nuestro acuario:
- El pH indica la acidez o alcalinidad del agua, basándose en la concentración de iones de hidrógeno cargados positivamente en una solución. Para medirlo, se utiliza una escala en la que el mínimo es “0” como ácido, “7” se considera neutro, y el máximo valor alcalino es “14”.
- El pH es un valor logarítmico y no lineal, por lo que, al medirlo, debemos ser tan precisos y exactos como nos permitan nuestros medios.
- El pH es sin duda el parámetro más importante del acuario, junto con la tasa de oxígeno disuelto y la temperatura, ya que afecta directamente al metabolismo de los organismos acuáticos a corto plazo.
- El pH afecta directamente a la toxicidad del amoníaco, por lo que es mucho más seguro permanecer en un pH ligeramente ácido en presencia de este compuesto nitrogenado.
- No todos los organismos acuáticos tienen la misma tolerancia a las alteraciones del pH. Debemos averiguar cuál es el gradiente máximo y mínimo al que están adaptados para evitar sobrepasarlo. Dentro de su propio gradiente, el metabolismo de los organismos sufre más por los cambios bruscos de pH que por permanecer en un extremo. Por ello, debemos ofrecerles tiempo suficiente para permitir su aclimatación. Como referencia, es aconsejable aumentar o disminuir medio punto de pH cada 24 horas. (F. Castelló Orvay, 1993)
- Es preferible medir, controlar y estabilizar el pH que preguntarse si los síntomas de un pez o un coral se deben a acidosis o alcalosis. ¿No estás de acuerdo?
- El método más práctico y económico para medir el pH es utilizar un kit de medición reactiva. Los lápices electrónicos de pH son muy recomendables a pesar de su precio más elevado. Es probable que cuesten menos dinero que los peces que mantenemos.
- La forma más segura y práctica de controlar y estabilizar el pH del acuario es utilizar acondicionadores comerciales de alta calidad. Podemos modificar directamente el pH del acuario, evitando provocar alteraciones demasiado bruscas, pero lo mejor es preparar la química del agua antes de realizar un cambio parcial.



